生命の設計図である染色体の維持と変化の分子メカニズムを解明
染色体DNAには生命の設計図が書き込まれています。そのため、細胞増殖に伴って、染色体の複製や分配が起きても、染色体は安定に維持されます。ただし、稀に、染色体の大きさや数が変化する染色体異常が起こることがあります。染色体異常は、癌などの遺伝病や細胞死を引き起こす要因となります。興味深いことに、染色体維持だけでなく、染色体異常も生体内の酵素が働くことで初めて起こります。我々の研究グループは、染色体維持と染色体異常、それぞれの分子メカニズムの解明と共に、その両者の「せめぎ合い」という生命の神秘を解き明かすことを目指します。
特色 FEATURE
新たな生命現象の発見とその分子メカニズムの解明を目指します
独創的な研究により新規研究領域の開拓を目指します
癌や自閉症などの診断や医療に資する研究を行います
成果 RESULTS
研究成果
DNA反復配列を「のりしろ」にした染色体異常の発生と抑制
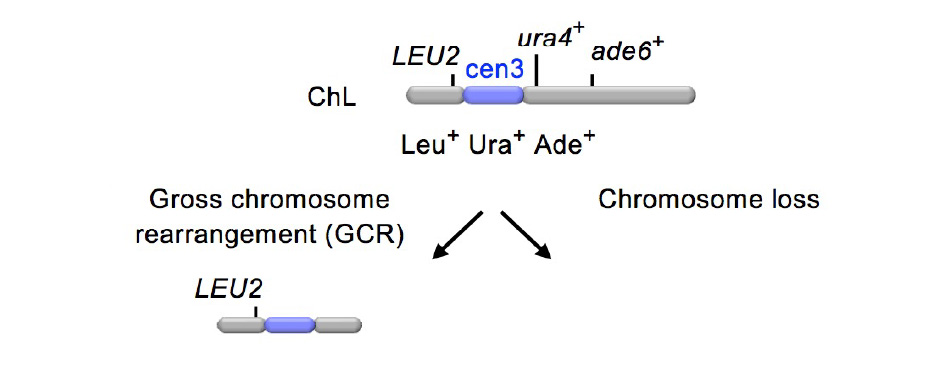
1)セントロメア反復配列を介した染色体異常の検出
本研究グループは、分裂酵母Schizosaccharomyces pombeを用いて、染色体異常の発生頻度を定量し、その構造を決定できる実験系を開発しました。染色体のセントロメア領域はDNA反復配列により構成されます。セントロメア反復配列を「のりしろ」にした染色体異常により形成される同腕染色体の検出に成功しました。
2)相同組換えによる染色体異常の抑制
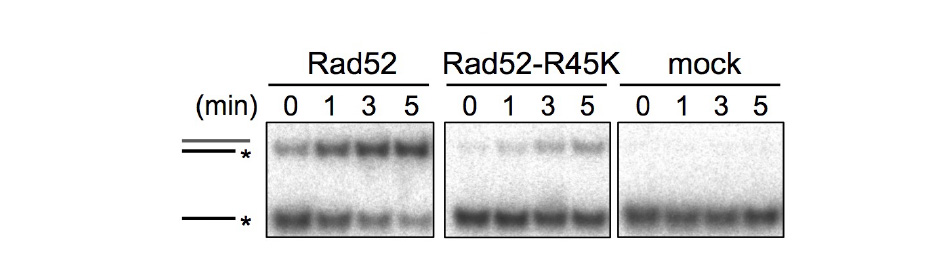
Rad51などが働くDNA相同組換えは、反復配列間での保守的組換えを促進することで、染色体異常を抑制することを明らかにしました。興味深いことに、他の染色体領域と比べて、セントロメア領域ではRad51による保守的組換えがより積極的に起きることを示しました。一方、Rad51が機能しない変異細胞では、別の組換え酵素Rad52などが働くことでセントロメア反復配列を介した染色体異常が起きることを明らかにしました。
3)ヘテロクロマチンによる転写阻害を介した染色体異常の抑制
細胞の核内では、DNAはヒストン蛋白などと相互作用することで様々なクロマチン構造を形成する。染色体クロマチンは、凝縮したヘテロクロマチン構造と弛緩したユークロマチン構造に大別される。セントロメアなど反復配列が存在する染色体領域は、ヘテロクロマチン構造を形成することで転写が阻害されています。ヘテロクロマチン構造を破壊すると、セントロメアでの転写が活発化し、その結果、染色体異常が起きることを明らかにしました。
今後の発展
染色体維持と染色体異常の分子メカニズムの解明
これまでの分子生物学により、染色体複製や染色体分配など個々の生命現象についての我々の理解は飛躍的に進みました。しかし、それらが実際に細胞内で、どのように互いに影響し合い、調和しているのかについての理解は今後の研究に委ねられています。染色体維持と染色体異常に関わるDNA複製、転写、組換え、クロマチン制御などについても同じに思われます。今後、これらの生命反応の間の連携を解き明かすことで、染色体の核心的な理解を目指します。特に、保守的組換えと染色体異常との関連や転写が染色体異常を誘発するメカニズムについて解析を進めます。